在腦機接口技術領域,電極作為連接生物神經系統與電子設備的核心組件,始終是制約技術突破的關鍵瓶頸。傳統植入式電極受限于“靜態”特性,植入后無法調整位置,且在長期使用中易引發免疫反應,導致信號衰減甚至失效。這一難題長期困擾著腦科學研究與應用發展,直到一項突破性成果的出現。
由中國科學院深圳先進技術研究院劉志遠、韓飛團隊聯合徐天添團隊,以及東華大學嚴威團隊歷時五年研發的“神經蠕蟲”(NeuroWorm)電極,為這一領域帶來了革命性變革。該成果發表于《自然》期刊,首次提出“動態電極”概念,通過引入磁控驅動技術,使電極能夠像生物蠕蟲般在體內自主移動,實現信號采集位置的動態調整。這一創新不僅突破了傳統電極的物理限制,更為腦機接口的精準監測與長期穩定性開辟了新路徑。
研究團隊的核心突破在于將磁性組件集成到超細纖維電極中。這種直徑僅196微米的電極,內部布局了60個獨立通道,相當于在頭發絲上雕刻出數十根精密導線。為實現這一目標,團隊采用了超薄柔性薄膜卷曲技術,結合導電圖案設計與軟硬接口優化,最終制備出可拉伸、耐疲勞的纖維電極。更關鍵的是,電極一端嵌入的微型磁頭允許通過外部磁場精確控制其運動方向,使其在體內實現厘米級精度的自主導航。
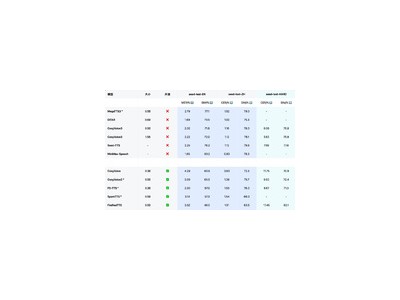
實驗數據顯示,NeuroWorm在兔子顱內成功完成了動態監測任務,能夠根據指令調整位置并持續采集高質量神經信號。這一特性在肌肉組織應用中表現尤為突出。團隊通過微創技術將電極植入大鼠腿部肌肉,發現其可在43周內穩定工作,且周圍組織形成的纖維包裹層厚度不足23微米,細胞凋亡率與正常組織無顯著差異。相比之下,傳統不銹鋼電極在相同條件下引發的包裹層厚度超過451微米,并伴隨明顯組織損傷。
“動態電極的研發涉及材料科學、微納制造、磁控技術等多學科交叉。”研究團隊成員指出,項目成功得益于跨領域協作。例如,徐天添團隊在磁驅動微型機器人領域的經驗,為電極運動控制提供了關鍵技術支撐;而劉志遠團隊在柔性電子領域的積累,則確保了電極的生物相容性與信號穩定性。這種多學科融合模式,正是當前腦機接口技術發展的核心驅動力。
值得注意的是,該研究不僅推動了基礎科學進步,更具備顯著的臨床應用潛力。在康復醫學領域,動態電極可實時監測肌肉運動狀態,為外骨骼設備提供精準控制信號;在神經疾病治療中,其長期穩定性與低免疫原性為癲癇、帕金森病等疾病的閉環調控提供了新工具。團隊此前開發的柔性可拉伸電極陣列已通過醫療器械認證,并實現量產供貨,標志著相關技術正加速向產業化過渡。
然而,研究團隊也清醒認識到技術挑戰。劉志遠研究員表示,未來需在驅動效率、材料壽命、功能集成等方面持續優化,例如探索更高效的磁控方式、開發自供能系統、提升電極與組織的融合度等。這些問題的解決需要全球科研力量的協同攻關,而“神經蠕蟲”的誕生無疑為這一進程奠定了重要基礎。